Jó hírt kaptak az Alzheimer-kórban szenvedők és az Eli Lilly részvényesei is
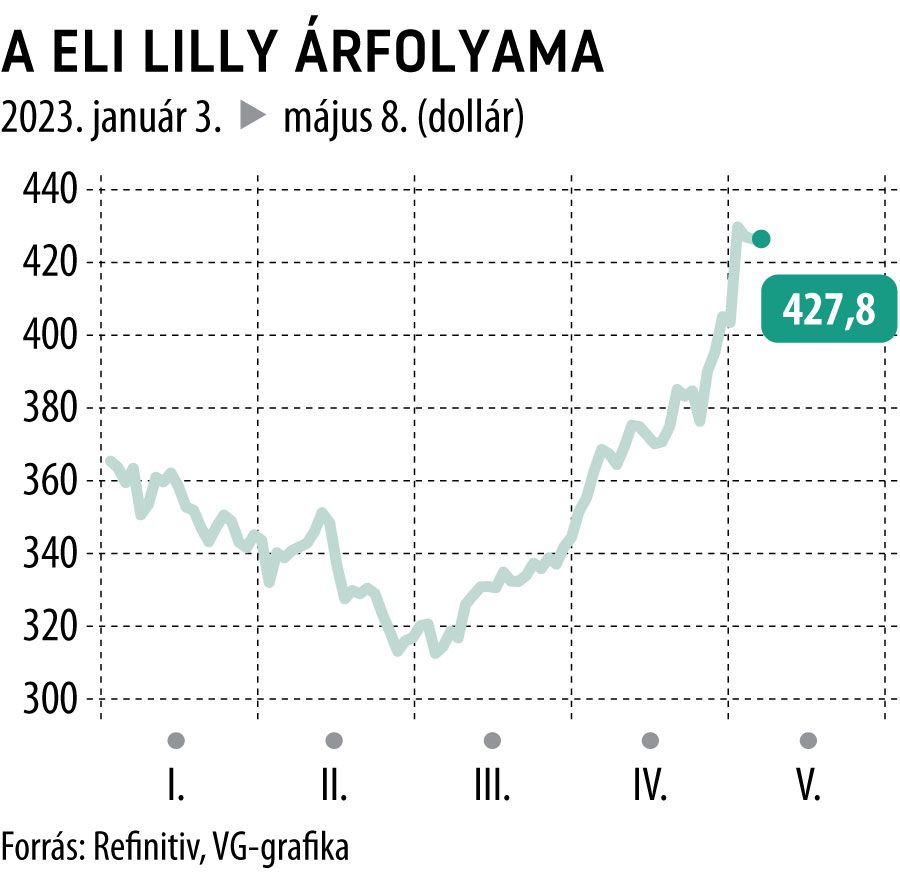
Közel 8 százalékkal, 428 dollárig lőtt ki az Eli Lilly részvényeinek árfolyama az elmúlt öt napban az amerikai gyógyszergyártó által az Alzheimer ellen kifejlesztett, kísérleti szakaszban lévő készítményről érkezett kedvező hírek nyomán.

A cég a múlt héten jelentette be, hogy
donanemab nevű hatóanyaga a placebóval kezelt betegekhez képest 35 százalékkal nagyobb arányban lassította a kognitív hanyatlást a harmadik fázisú klinikai vizsgálat adatai szerint. A kezelés 12. hónapját követően a betegek 47 százalékánál elmaradt a kór progressziója, szemben a placebocsoport 29 százalékos eredményével.
Az adatok újfent igazolják, hogy az agyban megtapadt amiloidplakkok eltávolítása előnyös a halálos kórban szenvedő betegek számára – vélik a szakértők.
A vizsgálatot 1182 olyan, korai stádiumban lévő betegnél végezték el, akiknek az agyában két kulcsfontosságú, a betegség progressziójával és az agysejtek pusztulásával összefüggő fehérje, a béta-amiloid, valamint a tau – az utóbbi közepes mértékben – rakódott le.
Ezenkívül a gyógyszert a kutatási eredményekről készült tanulmány 552 olyan betegnél is értékelte, akiknél a tau szintje kifejezetten magas volt, és megállapította, hogy a két csoport átlagában a donanemab 29 százalékkal lassította a demencia progresszióját az általánosan használt CDR-SB skálán (Clinical Dementia Rating Scale).
Az Eli Lilly eredményei valamivel jobbak, mint szektortársai, a japán Eisai és az amerikai Biogen közös fejlesztésű, Leqembi márkanév alatt forgalmazott gyógyszeréé, amely egy tavaly közzétett tanulmány szerint 27 százalékkal csökkentette a kognitív hanyatlást a korai fázisú betegeknél.
Az eredmény megint csak arra utal, hogy ezeket a plakkokat minél korábban el kell távolítani, mielőtt a tau igazán beindulna
– idézi a Reuters dr. Erik Musiek neurológust, a Washingtoni Egyetem specialistáját.
Vannak azonban egészségügyi kockázatai is az új gyógyszernek – akárcsak a Leqembinek és a Biogen által fejlesztett Aduhelmnek –, hiszen a donanemabbal kezelt páciensek 24 százalékánál agyduzzanat jelentkezett, ami a résztvevők 6,1 százalékánál tünetekkel is járt. A Lilly szerint az esetek 1,6 százalékban voltak súlyosak, beleértve két halálesetet is.
A donanemabcsoport 31,4 százalékánál és a placebocsoport 13,6 százalékánál pedig agyvérzést diagnosztizáltak.
A donanemab sikeres lehet, de a rizikófaktor is aggodalomra ad okot
– kommentálta a tanulmányt David Risinger, az SVB Securities elemzője.
A Leqembi 3. fázisú vizsgálatában a résztvevők közel 13 százalékánál állapítottak meg agyduzzanatot.
Az Eli Lilly gyógyszere lehet tehát a harmadik, Alzheimer-kezelésre alkalmas orvosság az amerikai piacon, ám figyelmeztető jel, hogy a Leqembi és az Aduhelm eddig nem bizonyult nagy sikernek, miután az orvosok és a biztosítók kevés bizonyítékot láttak kedvező hatásukra. Ráadásul mindkét készítményt gyorsított eljárásban engedélyezték.
Mindenesetre a Lilly közölte, hogy június végéig benyújtja a hagyományos – tehát nem gyorsított eljárásban kiadott – amerikai engedély iránti kérelmét, a jóváhagyást pedig legkésőbb 2024 elejére várják.
Az árazás a konkurenciáéhoz igazodik majd – árulta el David Ricks vezérigazgató a CNBC-nek.
Csak az Egyesült Államokban több mint 6 millióan élnek Alzheimer-kórral, és ez a szám 2050-re várhatóan közel 13 millióra emelkedik.
Az Eli Lilly részvényeit a Refinitiv elemzői konszenzusa 430 dolláros medián célárral javasolja vételre.








